Como virus de ARN, la replicación del genoma del SARS-CoV-2 es innatamente propensa a errores, por lo que se esperan mutaciones (1). De vez en cuando, una mutación proporcionará una ventaja adaptativa (como una mayor transmisibilidad o infectividad a un huésped humano) y será seleccionada positivamente en la población. Este proceso impulsa la evolución del genoma viral y da lugar a la rica diversidad de cepas y linajes virales que vemos. Sin embargo, para el SARS-CoV-2, la aparición inesperada de tal diversidad desde finales de 2020 ha generado una ansiedad considerable en torno a la progresión de la enfermedad y la eficacia de los diagnósticos y las vacunas para controlar su propagación.
El 22 de abril, Public Health England publicó la actualización 9 de SARS-CoV-2 Variants of Concern (VOC) y Variants Under Investigation (VUI) en England-Technical briefing. Una buena noticia es que no hay variantes conocidas de alto impacto (VOHC) en circulación hoy en día. Este informe técnico es un gran recurso para comprender las variantes emergentes. Se ha informado mucho en las noticias (2,3) sobre una variante «doble mutante» en la India, por lo que estaba ansioso por leer más sobre esta cepa B.1.617.1: su perfil genómico, filogenia y caracterización biológica en el información técnica.
Me impresionó la familiaridad de las mutaciones en la variante India B.1.617. Estos son el mismo «elenco de caracteres» que hemos visto en otras cepas variantes de interés, mutaciones en las mismas posiciones de aminoácidos que siguen apareciendo, ya sea en diferentes combinaciones o como diferentes sustituciones de aminoácidos.
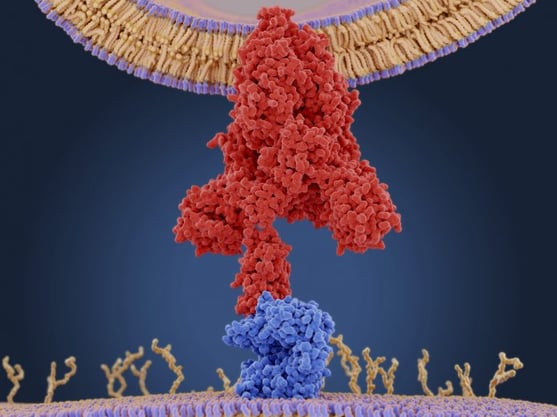
Figura 1: Modelo molecular de la proteína espiga (S) (roja) unida a un receptor ACE2 (azul) en una célula humana. Imagen tomada de (4). Si bien surgen mutaciones que definen el linaje en todo el ARN genómico del SARS-CoV-2 que afecta a todas las proteínas virales, hasta ahora, principalmente, solo las mutaciones en el gen Spike han surgido repetidamente en linajes independientes. Las mutaciones E484 y L452 discutidas en la variante B.1.617 India están en la superficie de la proteína espiga que en realidad hace contacto con el receptor ACE2.
En el ejemplo de la variante B.1.617 India:
- Mutación en la posición de Spike E484: Las mutaciones en esta posición se caracterizaron previamente en las variantes VOC-20DEC-02 (B.1.351 «Sudáfrica») y VOC-21JAN-02 (P.1 «Japón/Brasil»). Las mutaciones E484K y, en menor medida, E484G/D/A/Y están implicadas en el escape antigénico, posiblemente a través de una mayor afinidad de unión al receptor ACE2 de la célula huésped humana (5). La nueva variante de VUI B1.617.1 India tiene E484Q en lugar del E484K, más ampliamente estudiado, y aún no se sabe cómo esta mutación afecta la unión de ACE2.
- La mutación en la posición de Spike L452: L452R también se observa en la variante de India B.1.617 y se encuentra en varias otras variantes previamente caracterizadas, incluida la «variante de California» B.1.429. Esta mutación también está asociada con el escape antigénico tanto de los anticuerpos monoclonales terapéuticos como de los antisueros convalecientes debido a la mayor afinidad de unión al receptor. Algunos estudios sugieren que la afinidad de unión mejorada aumenta la capacidad de los virus para infectar células humanas y, por lo tanto, mejora la transmisibilidad (6).
- Mutación en el sitio de escisión de furina – Posición de espiga P681: B.1.617 La variante de India contiene la mutación del sitio de escisión de furina P681R, similar a P681H. Las mutaciones 681R/H se encuentran en múltiples linajes variantes, como VOC-20DEC-01 (B.1.1.7 «variante del Reino Unido»), variantes preocupantes del SARS-CoV-2 y variantes bajo investigación VUI-21FEB-04 (B. 1.1.318) y VUI-21FEB-01 (A.23.1). Tanto P681H como P681R optimizan la escisión de la espiga por furina, lo que puede mejorar la transmisibilidad del virus.
Estos ejemplos en la variante B.1.617 India no son únicos. La posición de la espiga Q677 ha mutado a H o P en al menos siete linajes diferentes, y los mutantes S-677 han aumentado la prevalencia alrededor de cinco veces en todo el mundo (7). De manera similar, la eliminación de picos ΔH69/V70 está presente en al menos 28 linajes de SARS-CoV-2 (8). Ahora, las variantes preocupantes (VOC) y las variantes bajo investigación (VUI) del SARS-CoV-2 en Inglaterra: el informe técnico 9 informa que, además de la mutación muy común N501Y que inicialmente definió la «variante del Reino Unido» B.1.1.7, ahora se está monitoreando una mutación N501T a partir de secuencias de Belo Horizonte, Brasil.
Las mismas mutaciones que aparecen una y otra vez sugieren una evolución convergente. La evolución convergente es cuando el mismo rasgo emerge en diferentes linajes independientes a lo largo del tiempo. La secuenciación del genoma a gran escala de virus de cientos de miles de pacientes (tal como están catalogados en la base de datos GSAID) permite identificar estos patrones convergentes. La mayoría de las mutaciones son eventos únicos que surgen en un paciente y se extinguen, pero algunas establecen nuevos linajes que se vuelven más frecuentes a medida que el virus logra replicarse e infectar a muchas personas (7). Se ha documentado que los pacientes inmunocomprometidos producen múltiples mutaciones con el tiempo (9). Estos nuevos linajes se identifican como VOC porque a menudo son responsables de los aumentos repentinos de COVID-19. Si las mutaciones en la misma posición de aminoácido surgen repetidamente en todo el mundo y se vuelven más frecuentes, esta mutación muy probablemente codifica una adaptación que ayuda al virus a reproducirse y transmitirse. Al observar las mutaciones definitorias en los linajes de VOC, podemos comprender qué posiciones son importantes para la aptitud viral.
Reflexionando sobre las variantes discutidas en este informe técnico, me sentí alentado porque parece haber una lista limitada de variantes que afectan la transmisibilidad y la virulencia viral. En lugar de un flujo interminable de nuevas variantes que son completamente impredecibles, la selección natural ya ha indicado las posiciones de aminoácidos que deben estar en nuestro radar para un seguimiento y una vigilancia estrechos.
El seguimiento y la vigilancia de las variantes emergentes se pueden realizar mediante ensayos de genotipado de RT-PCR basados en sondas de alto rendimiento o utilizando la secuenciación del genoma completo (NGS). Independientemente del método, las pruebas de vigilancia de variantes requieren el uso de materiales de control de calidad para optimizar los ensayos, garantizar la sensibilidad y monitorear el control de calidad diario. LGC SeraCare produceMateriales de referencia de SARS-CoV-2 que utilizan la tecnología patentada AccuPlex™. Estas partículas virales recombinantes están completamente encapsuladas como el patógeno SARS-CoV-2, por lo que deben pasar por un proceso de extracción antes de la detección del ácido nucleico, pero las partículas virales tienen defectos de replicación para un manejo seguro. Los materiales de referencia de la variante AccuPlex SARS-CoV-2 están actualmente en desarrollo. Los materiales contendrán el ARN genómico completo del SARS-CoV-2 y, para el primer lanzamiento del producto, se centrarán en las mutaciones del gen S en tres variantes destacadas de interés (Tabla 1).
| Cambio de aminoácidos | Cambio de nucleótido | B.1.1.7 variante del Reino Unido | B.1.351 Variante de África del Sur | P.1 variante Japón/Brasil |
| L18F | C21614T | X | ||
| T20N | C21621A | X | ||
| P26S | C21638T | X | ||
| Supresión HV 69-70 | 21765-21770 eliminación | X | ||
| D80A | A21801C | X | ||
| D138Y | G21974T | X | ||
| Eliminación Y144 | 21991-21993 eliminación | X | ||
| R190S | G22132T | X | ||
| D215G | A22206G | X | ||
| 242_244 DelLAL | 22286-22294 Del | X | ||
| K417N | G22813T | X | ||
| K417T | A22812C | X | ||
| E484K | G23012A | X | X | |
| N501Y | A23063T | X | X | X |
| A570D | C23271A | X | ||
| D614G | A23403G | X | X | X |
| H655Y | C23525T | X | ||
| P681H | C23604A | X | ||
| A701V | C23664T | X | ||
| T716I | C23709T | X | ||
| S982A | T24506G | X | ||
| T1027I | C24642T | X | ||
| D1118H | G24914C | X | ||
| V1176F | G25088T | X |
El kit tiene un vial para cada una de las tres variantes, así como un cuarto vial de control de tipo salvaje (secuencia de referencia NC_045512).
Con pruebas eficientes y de alta calidad para las variantes, combinadas con una comprensión más profunda de las posiciones críticas de los aminoácidos para una mayor aptitud viral, las comunidades pueden reaccionar a las nuevas cepas de manera adecuada y, cuando sea necesario, implementar medidas de cuarentena de manera más efectiva.
Infórmate sobre otros temas con nuestro blog. Visita nuestras redes sociales para más información